
MRD的概念最初指血液肿瘤中运用传统检测手段(例如流式细胞仪或PCR)检测残留的肿瘤细胞,即可测量的残留疾病(measurable residual disease)或微小残留病灶(minimal residual disease)。在分子水平检测的MRD也被称为molecular residual disease,主要检测循环肿瘤DNA(ctDNA)。
2017年在非小细胞肺癌患者临床研究中,报道了ctDNA能早于影像学手段检出肿瘤复发[1,2],自此,ctDNA作为疗效评估和复发预测的新兴生物标志物在实体瘤中受到越来越多的关注。我国每年的新发膀胱癌患者中,肌层浸润性膀胱癌(MIBC)约占20%;目前根治性膀胱切除是治疗MIBC的标准疗法,但50%的患者可能会在术后2年内复发。因此,MRD在膀胱癌预后诊断中具有十分重要的临床价值。
在此,结合本次2022 ASCO-GU学术会议上的最新报道,和大家一起深度探讨基于ctDNA的MRD检测应用于膀胱癌临床实践中的最新进展。
IMvigor010(NCT02450331)是一项探究接受根治治疗的尿路上皮癌患者能否从atezolizumab一线辅助治疗中获益的III期临床研究,结果显示在atezolizumab组和对照组间不存在显著差异。基于该研究纳入的患者,研究者通过在患者术后不同时间点检测血浆游离DNA,发现基线ctDNA阳性患者的复发风险显著增加(DFS HR=6.3),atezolizumab组ctDNA清除率显著高于观察组,且基线ctDNA阳性的患者可以从atezolizumab辅助治疗中获益[3],提示血浆ctDNA可以作为预测患者复发风险和能否从atezolizumab辅助治疗中获益的生物标志物。
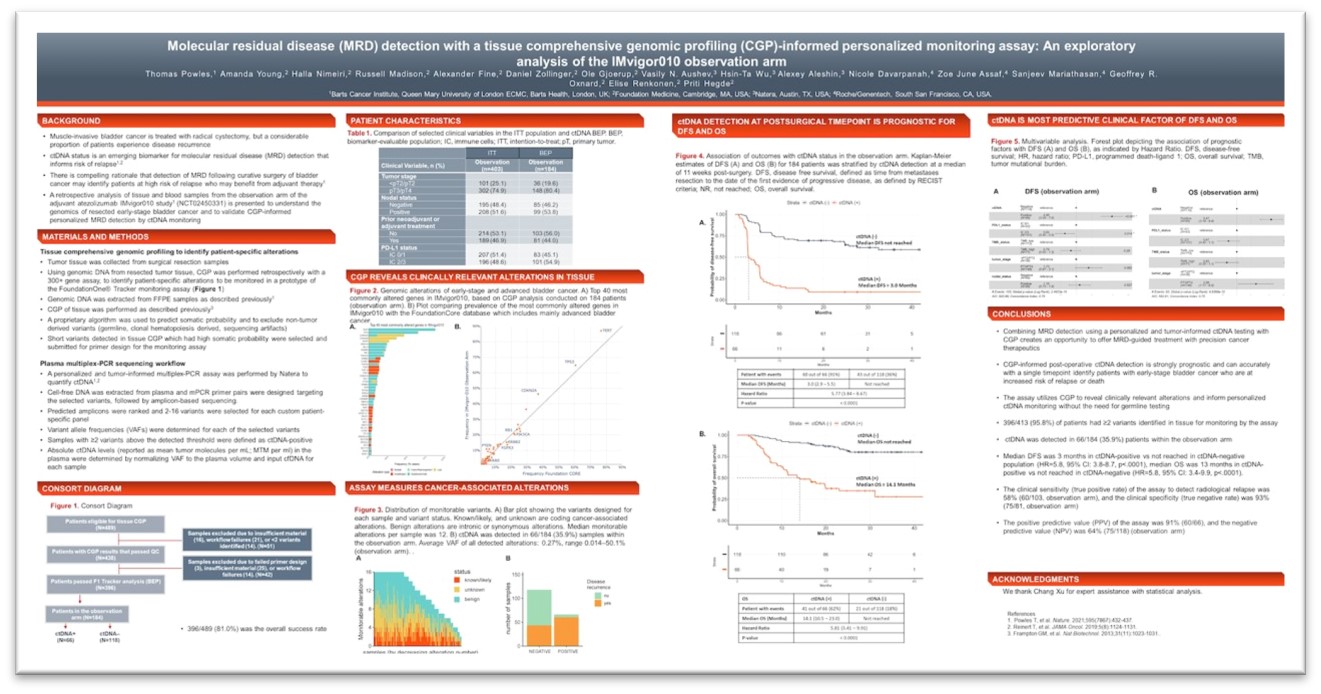
在本次2022 ASCO-GU会上,研究者进一步公布了基于IMvigor010临床试验的最新研究进展。该研究中,对489例接受根治术的患者进行了肿瘤组织依赖的定制化MRD检测。手术后第11周时,在66例MRD 检测为ctDNA阳性(≥2突变被认为ctDNA阳性)的患者中,58例患者复发(PPV=88%);生存分析显示,ctDNA阳性患者的DFS和OS显著短于ctDNA阴性患者(118例)。该研究证明基于肿瘤组织的定制化MRD检测可以作为评估患者术后复发风险和预后的生物标志物。
同样在本次会议上,上海交大仁济医院陈海戈教授团队公布了与慧渡医疗的一项合作研究结果。该研究采用了慧渡医疗推出的新一代定制化MRD检测产品PredicineBEACON™,可以在无法获得基线肿瘤组织的临床场景下,采用血浆或尿液作为基线样本,通过挑选50个患者特异的体细胞突变,结合具有临床价值的突变位点和拷贝数检测共同设计个体化MRD panel,从而进行疗效监控。基于cfDNA的性能验证研究显示当ctDNA含量高于0.005%,其敏感性可达100%,特异性>99%。
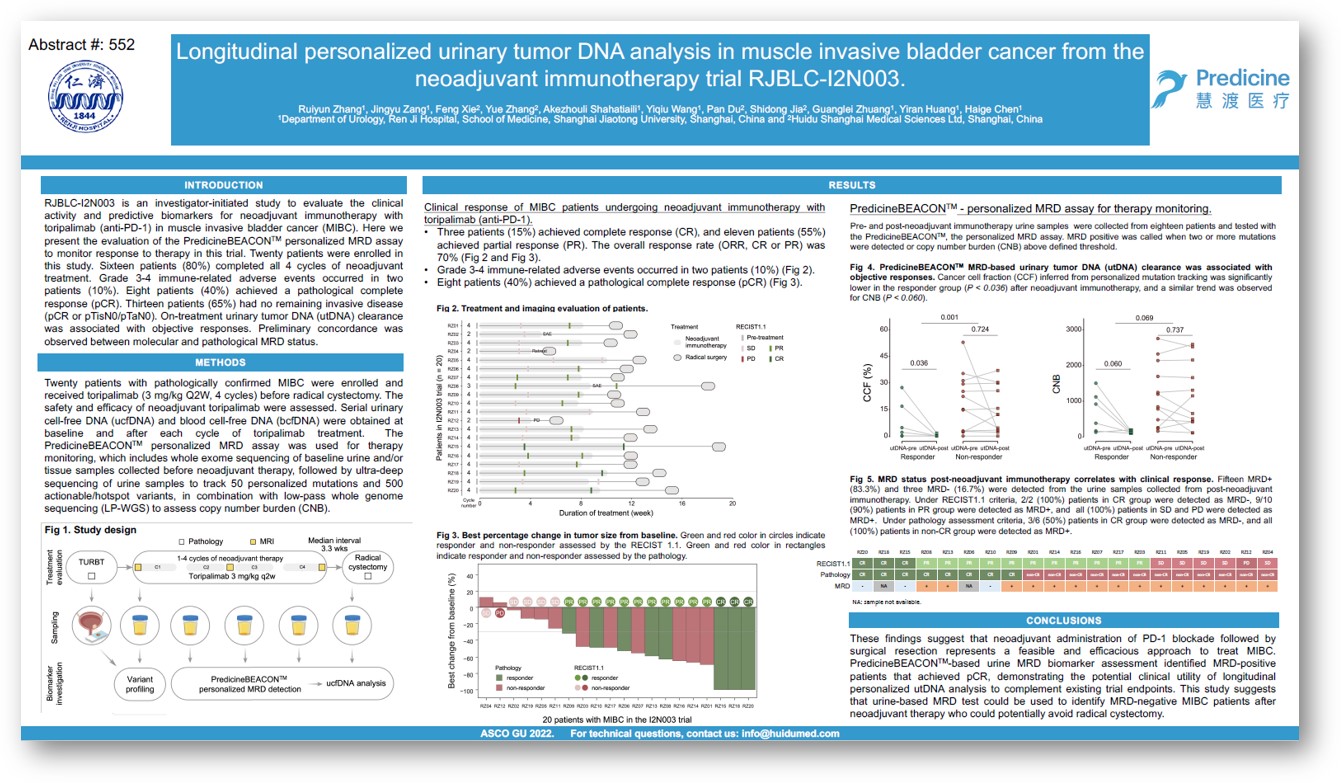
在早期纳入的完成了4个周期PD-1抑制剂toripalimab新辅助免疫治疗的18例MIBC患者中,基于尿液样本的PredicineBEACON™检测与患者的临床获益情况一致,显示该定制化MRD检测具有很高的临床应用价值。
此外, natera也在本次会议上分享了其MRD产品应用于三例膀胱癌患者新辅助治疗疗效评价、术后辅助治疗决策和长期的复发监测中的成功经验,初步肯定了定制化MRD作为新型分子标志物在临床管理中的价值。
以上研究初步证实了基于肿瘤组织,血浆或尿液样本中的ctDNA进行定制化MRD检测用于评估膀胱切除术疗效,膀胱癌患者预后及术后复发风险,预测辅助治疗和新辅助免疫治疗疗效的可行性。与需要提供肿瘤组织的MRD产品相比,慧渡医疗的PredicineBEACON™产品实现了不依赖肿瘤组织,仅仅利用血液或尿液样本就实现了患者的定制化MRD检测。尽管目前MRD在实体瘤中的临床应用还存在一些亟待解答的问题,但随着MRD检测的价值在越来越多的临床研究中得到证实,今后必将有更多的膀胱癌患者从其临床应用中获益。
References:
[1] Chaudhuri AA, Chabon JJ, Lovejoy AF, et al. Early Detection of Molecular Residual Disease in Localized Lung Cancer by Circulating Tumor DNA Profiling. Cancer Discov. 2017 Dec; 7(12): 1394-1403. doi: 10.1158/2159-8290. CD-17-0716. Epub 2017 Sep 24. PMID: 28899864; PMCID: PMC5895851.
[2] Abbosh C, Birkbak NJ, Wilson GA, et al. Phylogenetic ctDNA analysis depicts early-stage lung cancer evolution. Nature.2017 Apr 26; 545(7655): 446-451. doi: 10.1038/nature 22364. Erratum in: Nature. 2017 Dec 20. PMID: 28445469; PMCID: PMC5812436.
[3] Powles T, Assaf ZJ, Davarpanah N, et al. ctDNA guiding adjuvant immunotherapy in urothelial carcinoma. Nature. 2021 Jul; 595(7867): 432-437. doi: 10.1038/s41586-021-03642-9. Epub 2021 Jun 16. PMID: 34135506.
