HR阳性HER2阴性乳腺癌是乳腺癌中患者比例最高的群体,内分泌治疗是这类患者系统治疗的基本方法。常见的内分泌治疗药物包括雌激素受体调节剂他莫昔芬、雌激素受体降解剂氟维司群和芳香化酶抑制剂(依西美坦、来曲唑、阿那曲唑)等。然而长期内分泌治疗之后,患者往往会面临耐药局面。
至今已报道的可能与内分泌治疗耐药或预后差相关的分子机制有ESR1基因突变、PI3K信号通路突变、HER2基因扩增、FGFR1基因扩增等[1]。近年来,随着国外和国内CDK4/6抑制剂(阿贝西利、哌柏西利、达尔西利)和PIK3CA抑制剂(阿培利司)的获批,靶向治疗联合内分泌治疗已分别被指南推荐用于局部晚期或转移性HR+/HER2-乳腺癌患者的一线和二线治疗。
总体而言,HR+/HER2-乳腺癌是乳腺癌各亚型中预后最好的,目前一线内分泌单独治疗后进展的HR+/HER2-乳腺癌患者,接受CDK4/6抑制剂联合内分泌治疗的OS约为50个月左右。
ER+乳腺癌早期依赖于雌激素对雌激素受体ER的激活。ER属于核激素受体超家族,主要包括ERα和Erβ两种亚型;其中ERα由ESR1基因编码。该基因主要包括N端结构域(N-terminal domain,NTD)、DNA结合域(DNA binding domain,DBD)和配体结合域(ligand binding domain,LBD)。
ESR1基因突变在原发性乳腺癌患者中的发生频率低于5%,而在转移性ER+乳腺癌患者中高达20-30%,这些患者通常都接受了长期的他莫昔芬或芳香化酶抑制剂治疗[2,3,4]。ESR1基因突变主要位于LBD区,其中以D538G和Y537S突变最常见[2]。携带ESR1 D538G或Y537S突变的晚期或转移性ER+患者单独接受芳香化酶抑制剂治疗的疗效和预后较差[3,4]。
目前正在开展多个口服雌激素受体调节剂/降解剂的临床试验,包括GDC-9545、lasofoxifene等;其中lasofoxifene已经初步显示针对ESR1突变的临床活性,并已获得FDA快速通道资格,目前正在芳香化酶抑制剂联合CDK4/6抑制剂治疗失败的且携带ESR1突变的ER+/HER2-晚期或转移性乳腺癌患者中开展疗效和安全性研究(NCT03781063、NCT04432454)。
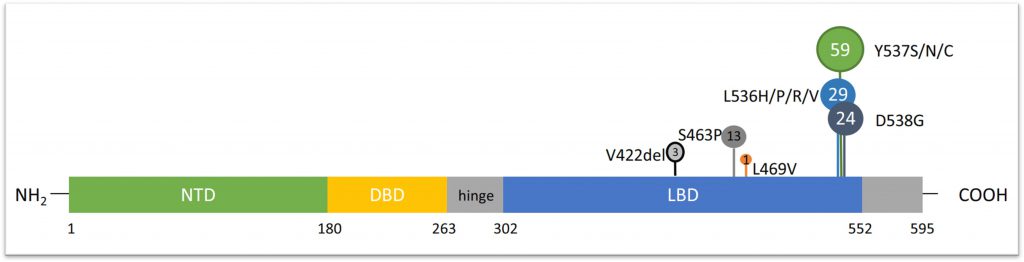
(图片来源于Gaillard SL, et al. Gynecol Oncol. 2019)
PI3Ks(phosphatidylino-sitol 3-kinases,磷脂酰肌醇-3-激酶)属于脂类的激酶,包括三类;其中I类激酶是由调节亚基p85和催化亚基p110构成的异二聚体,p110由PIK3CA基因编码。
在细胞膜上的生长因子受体或G蛋白偶联受体被来自细胞外的配体激活后,PI3Ks催化膜脂磷脂酰肌醇-4,5-二磷酸PI(4,5)P2生成第二信使PI(3,4,5)P3,PI(3,4,5)P3依赖的激酶PDK1激活关键激酶AKT,AKT进而磷酸化众多底物,继而引起下游一系列信号通路的转导。PTEN基因编码一个磷酸酶,可以将PI(3,4,5)P3去磷酸化生成PI(4,5)P2。PI3K/AKT/PTEN通路对于调节细胞的增殖、分化、凋亡以及迁移十分重要。
有研究报道在高达40%的ER+/HER2-乳腺癌患者中可检出PIK3CA基因突变,其中以螺旋结构域的E545K和E542K突变和激酶结构域的H1047R突变最为常见[5,6,7]。相比之下,PTEN和AKT1/2/3基因在这类患者中的突变频率很低,其中AKT1基因的热点突变E17K的突变频率约为3%[8]。
目前,已经有大量针对该信号通路分子开发的抑制剂,其中FDA已经批准mTOR抑制剂依维莫司(everolimus)用于HR+/HER2-乳腺癌患者,批准小分子PI3Kα特异性抑制剂阿培利司(alpelisib)联合氟维司群用于携带PIK3CA突变的HR+/HER2-乳腺癌患者,其他抑制剂则正在乳腺癌和其它实体瘤中开展临床试验,如泛PI3K抑制剂copanlisib(NCT02465060)、PI3Kα特异性抑制剂GDC-0077(NCT03006172)、AKT抑制剂AZD5363(NCT03772561)等。
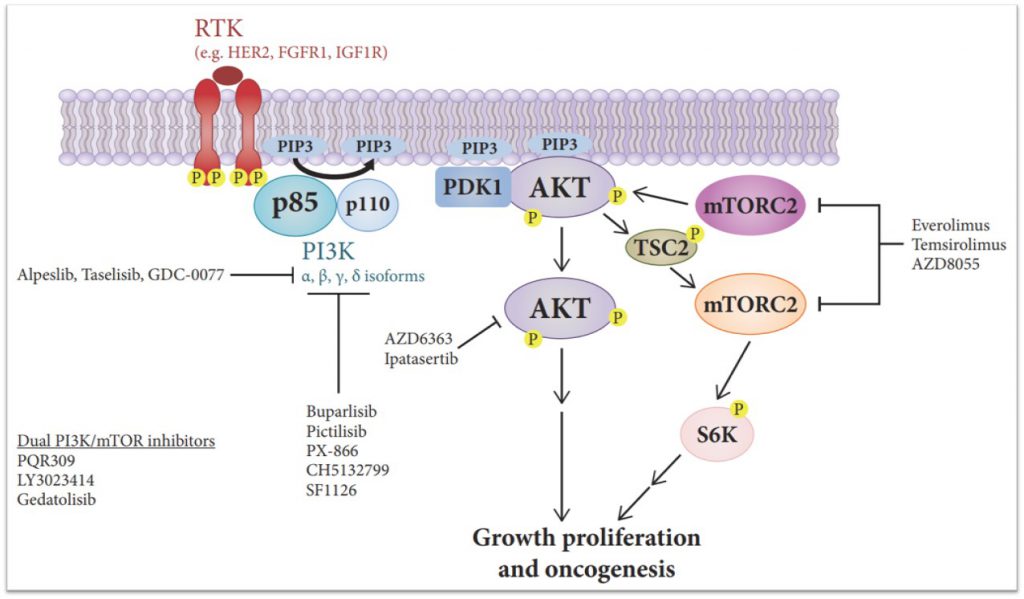
(图片来源于Vasan N, et al., Ann Oncol. 2019)
作为新一代液态活检精准医疗国际领军企业——慧渡医疗,针对以上基因自主研发的针对外周血的液态活检产品和MRD检测产品,具有灵敏度高和样本量要求量低的优势。在乳腺癌领域,已经与北京大学肿瘤医院、美国西北大学、美国华盛顿大学等知名机构和多家国际顶尖药企开展了临床合作研究和药物注册研究,并取得丰硕研究成果(点击查看原文Journal of Translational Medicine,
Frontiers in Oncology,ESMO 2022),为新一代液态活检技术服务全球乳腺癌患者,为个体化治疗打下了坚实的基础。
参考文献:
[1] Hanker AB, Sudhan DR, Arteaga CL. Overcoming Endocrine Resistance in Breast Cancer. Cancer Cell. 2020 Apr 13;37(4):496-513. doi: 10.1016/j.ccell.2020.03.009. PMID: 32289273; PMCID: PMC7169993. [2] Toy W, Weir H, Razavi P, et al. Activating ESR1 Mutations Differentially Affect the Efficacy of ER Antagonists. Cancer Discov. 2017 Mar;7(3):277-287. doi: 10.1158/2159-8290.CD-15-1523. Epub 2016 Dec 16. PMID: 27986707; PMCID: PMC5340622. [3] Chandarlapaty S, Chen D, He W, et al. Prevalence of ESR1 Mutations in Cell-Free DNA and Outcomes in Metastatic Breast Cancer: A Secondary Analysis of the BOLERO-2 Clinical Trial. JAMA Oncol. 2016 Oct 1;2(10):1310-1315. doi: 10.1001/jamaoncol.2016.1279. Erratum in: JAMA Oncol. 2019 Jan 1;5(1):122. PMID: 27532364; PMCID: PMC5063698. [4]Fribbens C, O’Leary B, Kilburn L, et al. Plasma ESR1 Mutations and the Treatment of Estrogen Receptor-Positive Advanced Breast Cancer. J Clin Oncol. 2016 Sep 1;34(25):2961-8. doi: 10.1200/JCO.2016.67.3061. Epub 2016 Jun 6. PMID: 27269946. [5]Vasan N, Toska E, Scaltriti M. Overview of the relevance of PI3K pathway in HR-positive breast cancer. Ann Oncol. 2019 Dec 1;30(Suppl_10):x3-x11. doi: 10.1093/annonc/mdz281. PMID: 31859348; PMCID: PMC6923788. [6]Zardavas D, Te Marvelde L, Milne RL, et al. Tumor PIK3CA Genotype and Prognosis in Early-Stage Breast Cancer: A Pooled Analysis of Individual Patient Data. J Clin Oncol. 2018 Apr 1;36(10):981-990. doi: 10.1200/JCO.2017.74.8301. Epub 2018 Feb 22. PMID: 29470143. [7]Razavi P, Chang MT, Xu G, et al. The Genomic Landscape of Endocrine-Resistant Advanced Breast Cancers. Cancer Cell. 2018 Sep 10;34(3):427-438.e6. doi: 10.1016/j.ccell.2018.08.008. PMID: 30205045; PMCID: PMC6327853. [8]Stemke-Hale K, Gonzalez-Angulo AM, Lluch A, et al. An integrative genomic and proteomic analysis of PIK3CA, PTEN, and AKT mutations in breast cancer. Cancer Res. 2008 Aug 1;68(15):6084-91. doi: 10.1158/0008-5472.CAN-07-6854. PMID: 18676830; PMCID: PMC2680495.
